公司新闻 山东淄博新达制药有限公司
生产管控——质量为先
发布时间:2020-09-28
生产管控——质量为先公司于8月28日-8月29日开展了为期两天的《质量控制体系提升和完善》线上培训活动,质量保证部及生产部相关人员参与了本次线上培训活动。

一、法规对MAH质量体系建设的要求,以及质量体系完善性评估。
药品上市许可持有人制度(MAH)是《药品管理法》确定的药品管理基本制度、核心制度,是药品安全的第一责任人。药品上市许可持有人依法对药品研制、生产、经营、使用全过程中药品的安全性、有效性和质量可控性负责。
二、偏差调查能力的提升。
偏差管理七步骤:偏差的汇报→评估→调查→纠正预防措施的制定→物料/产品评估→偏差报告的批准→纠正预防措施的跟踪落实。
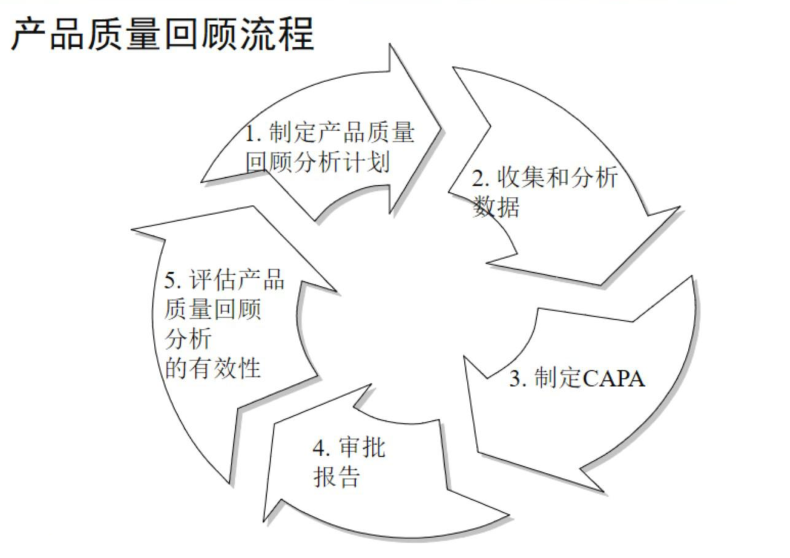
三、CAPA实施方法的提升。
系统的、标准的和有效的CAPA可以提高产品过程能力,减少检查中的不良发现,是解决质量和法规符合性问题或风险所需要的一系列行动的集合和管理措施。
四、员工资质评估、培训的管理。
岗前培训和继续培训。岗前培训是常规且涉及相关基本技能。继续培训应长期的,有计划的:适应最新法规要求的培训;满足实际培训需求的培训;关键人员的特殊培训;重点标准操作规程的重复培训;偏差分析及预防措施等。
五、文件、记录控制。
文件起草→文件审核→文件批准→文件培训→文件生效→文件发放→文件补发→文件执行和填写→文件变更/修订→文件收回→文件储存→文件销毁。
六、变更管理。
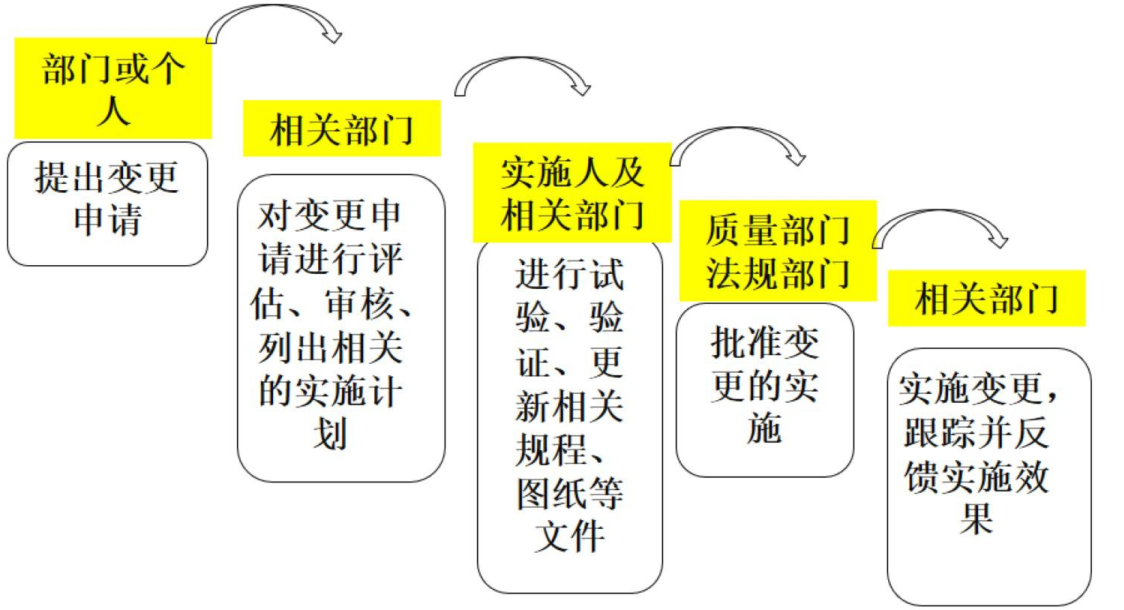
投诉:接收客户投诉→影响评估→调查→调查结论的批准和纠正及预防措施的确认→纠正及预防措施的追踪及结案。
召回:评估产品事故→产品召回的决定→通知销售部门→起草召回方案→实施召回方案。召回的模拟颜料:如上一年度没发生过召回,应每年根据药品召回模拟方案测试药品召回,测试应包括药品召回决定过程,而不局限于库存的追踪。
九、供应商管理、委托生产、销售管理。
十、自检与放行专题。
自检:制定自检计划→准备自检→自检→完成报告。
放行:生产放行和上市放行。


- 上一篇:苦练三伏砺精兵,实战竞训强技能
- 下一篇:2020年版《中国药典》网络宣传贯彻会议



